Una investigación con participación de investigadores del
CIBERNED del Instituto de Salud Carlos III (ISCIII), ha demostrado la viabilidad y seguridad de la introducción de terapia génica con vectores virales en el cerebro de primates de manera focal y no invasiva, gracias a la apertura temporal de la barrera hematoencefálica mediante ultrasonidos de baja intensidad (LIFU) en regiones relevantes para el estudio de pacientes con enfermedad de Parkinson. El estudio, cofinanciado por el ISCIII, está coordinado desde el Centro Integral de Neurociencias AC HM CINAC, ubicado en el Hospital Universitario HM Puerta del Sur de Móstoles, en Madrid.
Los resultados obtenidos en este trabajo abren la puerta a nuevos escenarios y representan un punto de partida para futuros ensayos con aplicación en otras enfermedades neurodegenerativas y tumores cerebrales. Los autores principales del artículo,
que se publica hoy en la revista Science Advances, son Javier Blesa y José Ángel Pineda-Pardo, investigadores de HM CINAC y del CIBERNED-ISCIII. En la investigación también han participado científicos de la Universidad de Kyoto (Japón).
El equipo de científicos de HM CINAC, CIBERNED-ISCIII y la Universidad de Kyoto, dirigidos por el profesor José A. Obeso, ha demostrado que es posible administrar un vector viral en el cerebro de manera focal y no invasiva en modelos animales. La introducción de vectores virales mediante apertura de la barrera hematoencefálica en zonas concretas del cerebro es un adelanto conceptual que representa un punto de partida para futuros ensayos de seguridad y eficacia en pacientes; los autores señalan que este avance posibilitará el diseño de nuevas estrategias terapéuticas personalizadas, en regiones concretas del cerebro, sin afectar al resto de estructuras cerebrales.
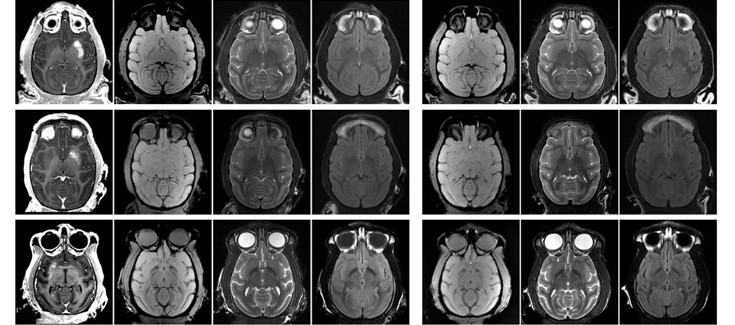
Los vectores virales se inyectaron a través de una vena periférica y penetraron al cerebro gracias a la apertura de la barrera hematoencefálica: "Es importante destacar que, al ser una apertura focal, los vectores virales llegan únicamente a la región en la que se ha actuado, evitando la interacción con el resto de las estructuras cerebrales, lo que permitirá en última instancia el diseño de estrategias terapéuticas personalizadas. En este estudio hemos demostrado que el suministro de terapia génica es seguro, sin daño visible en el cerebro", señala el Dr. Pineda-Pardo en referencia a los modelos animales utilizados.
En concreto, se logró la administración vía intravenosa de adenovirus tipo 9 a regiones del cerebro afectadas en la enfermedad de Parkinson, sin que se observaran efectos secundarios negativos, ni daños en los tejidos. El estudio sugiere que esta administración podría generalizarse a otros vectores virales utilizados en terapia génica, y abre la puerta a posibles avances en Parkinson, Alzheimer, Huntington o esclerosis lateral amiotrófica gracias al uso de moléculas que podrían llegar al cerebro de forma más eficiente con este tipo de procedimiento.
Referencia del artículo:
Javier Blesa et al. BBB opening with focused ultrasound in nonhuman primates and Parkinson’s disease patients: Targeted AAV vector delivery and PET imaging. Sci. Adv.9, eadf4888(2023). DOI:10.1126/sciadv.adf4888.